MONOGRAFÍA DEL PRODUCTO
NOMBRE DEL PRODUCTO:
MILENIUM® (ESOMEPRAZOL) 20 MG Y 40 MG CÁPSULA CON PELLETS ENTERICOS
QUALIUM® (ESOMEPRAZOL) 20 MG Y 40 MG CÁPSULASCON PELLETS ENTERICOS
QUÍMICA DEL PRINCIPIO ACTIVO
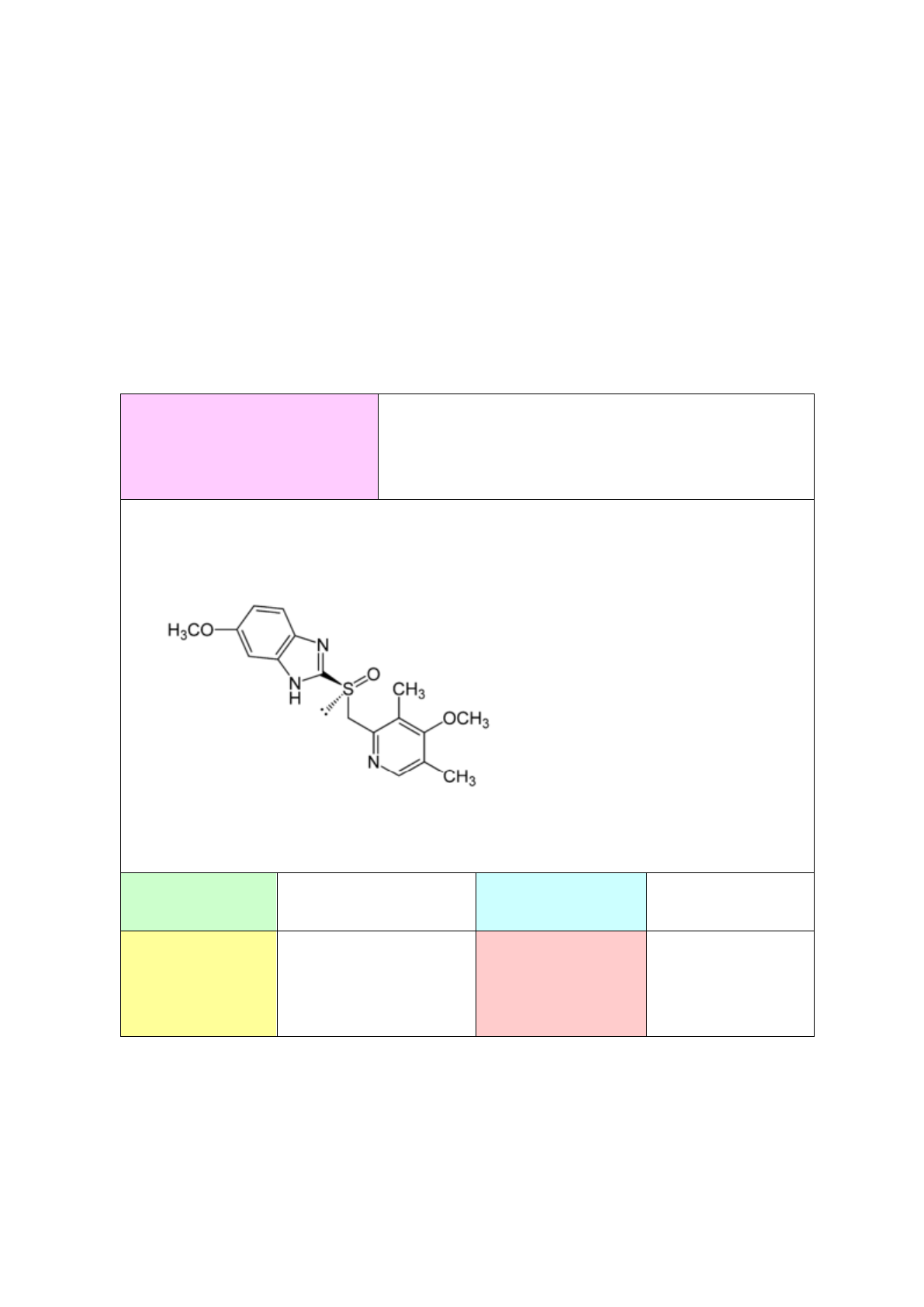
Nombre químico
(S)-5-metoxi-2-[(4-metoxi-3,5-dimetilpiridin-2-il)
metilsulfinilo]-3H-benzoimidazol
Fórmula
C17H19N303S
Peso
Molecular
[g/mol]
345,416
Número CAS
119141-88-7
Código ATC
A02BC05
A02BC01
NOMBRE DEL MEDICAMENTO
Milenium 20 mg Cápsulas con Pellets Entéricos
Milenium 40 mg Cápsulas con Pellets Entéricos
Qualium 20 mg Cápsulas con Pellets Entéricos