Monografía de producto
Departamento Médico y Regulatorio
Acepress® tabletas recubiertas Irbesartan 300 mg
Acepress® tabletas recubiertas Irbesartan 150 mg
ACEPRESS®
Irbersartan
Tabletas recubiertas
Vía Oral
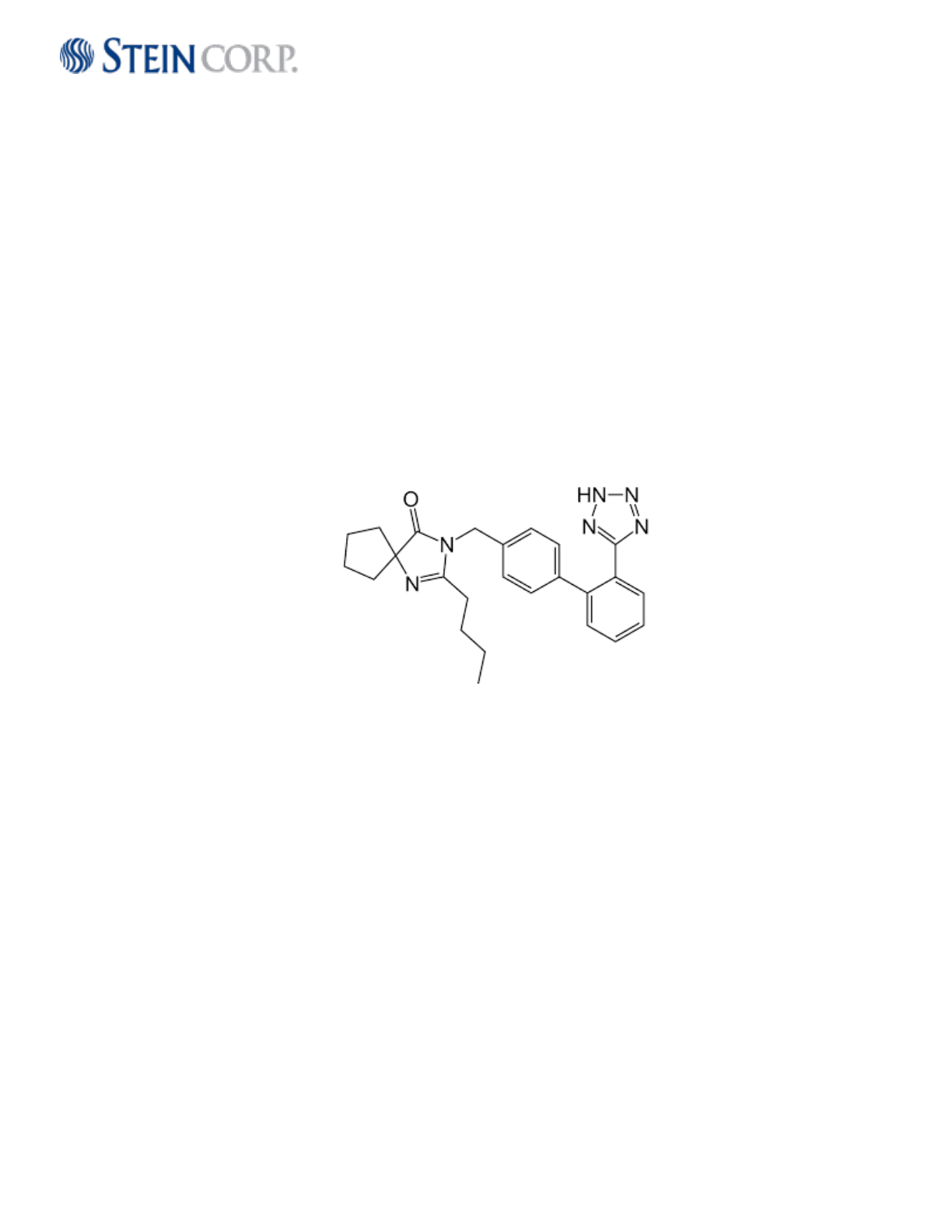
Nombre IUPAC: 2-butyl-3-[[4-[2-(2H-tetrazol-5-yl)phenyl]phenyl]methyl]-1,3-
diazaspiro[4.4]non-1-en-4-one
Código ATC: C09CA04
Estructura química:
CATEGORÍA FARMACOLÓGICA
Antagonistas de angiotensina-II, monofármacos.
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada tableta recubierta contiene 150mg o 300mg de irbesartán.
Lista de excipientes: lactosa monohidratada, croscarmelosa sódica, crospovidona, dióxido
de silicio coloidal, poloxamer 188 A, estearato de magnesio, agua desionizada,
metiletilcelulosa, lactosa monohidratada, metilparabeno, polietilenglicol 8000, sacarina,
talco simple.
DATOS CLÍNICOS
Indicaciones terapéuticas